От Большого взрыва до молекулярного транзистора: краткая история углерода
Дмитрий Борисов — о книге Роберта Хейзена «Симфония № 6»
Роберт Хейзен. Симфония № 6. Углерод и эволюция почти всего. М.: Альпина нон-фикшн, 2021. Перевод с английского Анастасии Науменко. Содержание

Симфо-минералогия
Минералог и астробиолог Роберт Хейзен, в честь которого назвали редкий минерал хазенит (сам Хейзен характеризует его не иначе как «фекалии микроорганизмов») до выхода на пенсию в 2016 году играл на трубе в Вашингтонской национальной опере и в Национальном симфоническом оркестре (общий музыкальный стаж — 44 года).
Его книга об углероде композиционно построена как классический четырехчастный цикл: каждая из частей симфонии связана с первоэлементами — Землей, Воздухом, Огнем, Водой (после выхода книги в 2019 году композитор Дэвид Эрл написал «Углеродную симфонию» — A Carbon Symphony, — которую исполнил Королевский шотландский национальный оркестр).
Первая часть — «Земля» — посвящена минералам и горным породам, Вселенной в целом и нашей планете в частности в пору их становления, когда атомы углерода образовывались из более мелких элементарных частиц. В главе «Воздух» рассказывается о глубинном углеродном цикле Земли, во время которого шестой элемент мигрирует из океана в атмосферу и обратно, проникает в недра Земли при движении литосферных плит и выбрасывается на поверхность с горячими газами вулканов. Раздел «Огонь» посвящен использованию углерода в энергетике, промышленности и наноинженерии — в производстве вагона и маленькой тележки полезных вещей и в создании инновационных технологий: от влагостойкой краски и сверхпрочного клея до углеродных нанотрубок и транзисторов из нескольких молекул. И, наконец, «Вода» — глава о происхождении и эволюции жизни.
Негибкие, высокомерные, инертные, взрывоопасные
Чтобы стать «первым парнем на деревне», а потом и «отцом родным» для множества форм, углерод должен был соответствовать ряду характеристик: в первую очередь, быть достаточно распространенным и доступным в земной коре, океане и атмосфере. Не инертным (не должен сидеть и ждать, когда другие элементы сами подойдут и предложат соединиться), но и не слишком «горячим парнем» (в смысле, не слишком химически активным — не самовозгораться и не взрываться при малейшем взаимодействии). Участвовать более чем в одной химической реакции, уметь образовывать прочные и стабильные связи, хранить и копировать информацию, а также использовать энергию от соединений с другими химическими элементами или энергию солнечного света.
Водород и гелий, самые распространенные в космосе элементы («партбилеты» № 1 и № 2 соответственно), на эту роль не годятся. Водород может крепко соединяться за раз только с одним атомом. Водородная связь играет важную роль в формировании жизни, выполняя функцию «молекулярного клея» — партнера кислорода в воде и посредника всех известных форм жизни. Но один водород обеспечить основу для жизни не в состоянии. Гелий — сноб, каких еще поискать, «невозможно инертный, высокомерный благородный газ», отказывающийся соединяться даже с самим собой.
Лития, бериллия и бора — № 3, 4, 5 — маловато будет. А вот про шестой номер — углерод, герой нашего, всех предыдущих и последующих времен, ради которого мы все здесь собрались (в прямом и в переносном смысле), — мы уже поняли, что он наше все.
Азот (элемент № 7) составляет около 80% атмосферы и связывается сам с собой в пары N2 — химически неактивные молекулы, представляющие бо́льшую часть газа, которым мы дышим. Также азот связывается и со многими другими элементами (среди них водород, кислород и углерод). Белки получаются из длинных цепочек аминокислот, каждая из которых содержит как минимум один атом азота. ДНК и РНК также содержат азот. Но химические реакции азота слишком энергичные, а возникающие связи слишком негибкие, чтобы он мог играть первую скрипку.
Кислород, несмотря на свое изобилие (его в земной коре в 1 000 раз больше углерода), химически скучен. Кислород является абсолютной основой всех биологически важных химических веществ — сахаров, аминокислот, воды. Но он не умеет формировать ни цепочек, ни колец, ни ветвящихся структур, которые нужны для сложной архитектуры жизни.
Фтор — № 9 Периодической таблицы, — будучи чрезвычайно химически активным, разъедает металл, протравливает стекло и взрывается при контакте с водой. Элементы № 10 и № 18, неон и аргон, — инертные газы. And so on, and so on...
Разве что кремний, элемент № 14, заметно отличается, что породило грезы о возможном существовании кремниевой жизни. Но и с ним ничего не получится.
«Кремний — это биологический тупик. У этого элемента на поверхности Земли есть только одна связывающая обязанность — найти четыре атома кислорода и образовать с ними кристалл. Эти раз и навсегда сформированные связи кремния с кислородом остаются слишком крепкими и негибкими, чтобы участвовать в интересной химии. Вы просто не можете основать биосферу на столь целеустремленном элементе, как № 14».
Еще выделяется в этом параде железо, элемент № 26, четвертый по распространенности в земной коре после кислорода, кремния и магния.
«Железо любит связываться, и оно гибкое в своем выборе. Соединяется ли с кислородом? Конечно: образует ржавчину с ионными связями. Соединяется ли с серой? Разумеется: создает сверкающий золотым металлическим блеском пирит (называемый, кстати, „золотом дураков”) с ковалентными связями. Железо связывается с мышьяком и сурьмой, хлором и фтором, азотом и фосфором, даже с углеродом в различных минералах карбида железа. А если других элементов под рукой нет, железо радостно связывается само с собой в виде самородного металла. <...> но у железа есть недостаток: оно с готовностью образует минералы с большими кристаллами, но избегает создавать маленькие молекулы. Жизнь требует огромного разнообразия молекул — в виде цепочек и колец, веток и решеток, — которые железо редко пытается образовать».
Так что остается углерод. Давайте посмотрим, когда и при каких обстоятельствах он появился.
 Роберт Хейзен
Роберт Хейзен
Минуты готовности
Составные элементы нашего мира берут начало в «17-минутном всплеске ядерного творчества» — процессе нуклеосинтеза Большого взрыва (НБВ). Большой взрыв — исключительное событие, случившееся 13,8 млрд лет назад, когда вся материя и энергия внезапно возникли в одной точке. Вселенная начала расширяться (это продолжается до сих пор), расширение дало охлаждение, а охлаждение принесло череду уплотнений (застываний) каскадов преобразований, каждое из которых сделало космос более организованным.
Первыми из невообразимо горячего и плотного вихря сконденсировались кварки (строительные блоки атомных ядер) и лептоны (их первое поколение — электроны). За первую секунду после Большого взрыва температура упала до ~ 100 трлн градусов — триплеты кварков соединились во множество протонов и нейтронов. Протонов оказалось больше (в соотношении примерно 7:1).
На третьей минуте во Вселенной создались благоприятные условия для образования стабильных атомных ядер (различных комбинаций протонов и нейтронов, удерживаемых вместе ядерными силами). Температура снизилась до ~ 100 млрд градусов.
Следующие 17 минут свободные нейтроны беспорядочно соединялись с протонами и формировали тяжелый изотоп водорода, называемый дейтерием. Большая часть атомов дейтерия затем попарно объединилась в изотоп гелия с двумя протонами и двумя нейтронами — гелий-4. На 20-й минуте ядерные частицы (протоны и нейтроны) соединялись во всевозможные комбинации, формируя, помимо прочего, небольшое, но важное количество гелия-3 (два протона плюс нейтрон) и лития-7 (три протона плюс четыре нейтрона), а также более крупные нестабильные ядра, которые быстро распадались.
Астрофизик Фабио Иокко из Южно-Американского института фундаментальной физики вместе со своими коллегами представил более сотни цепочек ядерных реакций, произошедших между третьей и 20-й минутой после Большого взрыва. Все эти реакции ранее не учитывались, поскольку считались чрезвычайно маловероятными. Исследователь уточняет: маловероятные не значит невозможные. По его мнению, и углерод, и азот, и кислород — все сформировались при НБВ. Но этих элементов тогда было очень мало. По вычислениям Иокко, примерно на каждые 4 500 000 000 000 000 000 (четыре с половиной квинтиллиона) ядер водорода появлялось одно ядро углерода.
«Однако крошечная доля огромного числа — это очень большое число. Простое деление показывает, что Большой взрыв произвел более 1 064 атомов углерода! Это количество представляет собой лишь малую долю массы Вселенной и лишь одну триллионную часть всех атомов углерода, обнаруженных во Вселенной сегодня, но первичных атомов углерода все же было много. <...> Поразительный вывод: бесчисленное множество атомов углерода вашего тела сформировалось не в звездах, как мы привыкли считать, а при Большом взрыве — целых 13,8 млрд лет назад, в начале времен. Известно изречение Карла Сагана: „Мы состоим из звездного пепла”. Но благодаря углероду НБВ мы также состоим из пепла Большого взрыва», — пишет Роберт Хейзен.
Слоеный пирог Земли
Мантия Земли разделена на три широкие сферические зоны. Нижняя мантия простирается с глубины ~ 670 км до границы ядра и мантии на глубине почти 2 900 км (занимает более половины объема Земли). Переходная зона — слой Голицына — образует оболочку на глубинах от 410 до 670 км. Верхняя мантия доходит почти до поверхности Земли. Внешние оболочки Земли (скорлупа, «тончайшие слои») в совокупности составляют менее 160 км (при радиусе Земли в 6 371 км; порядка 1% массы планеты).
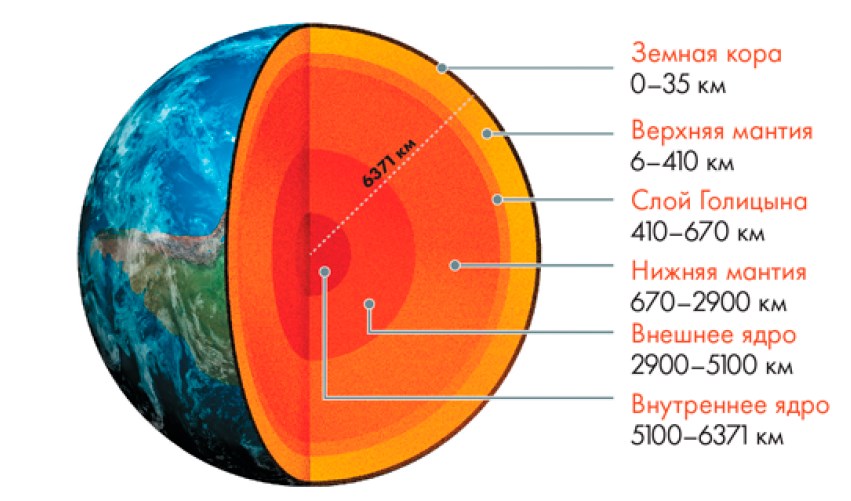 Рисунок из книги (с. 362)
Рисунок из книги (с. 362)
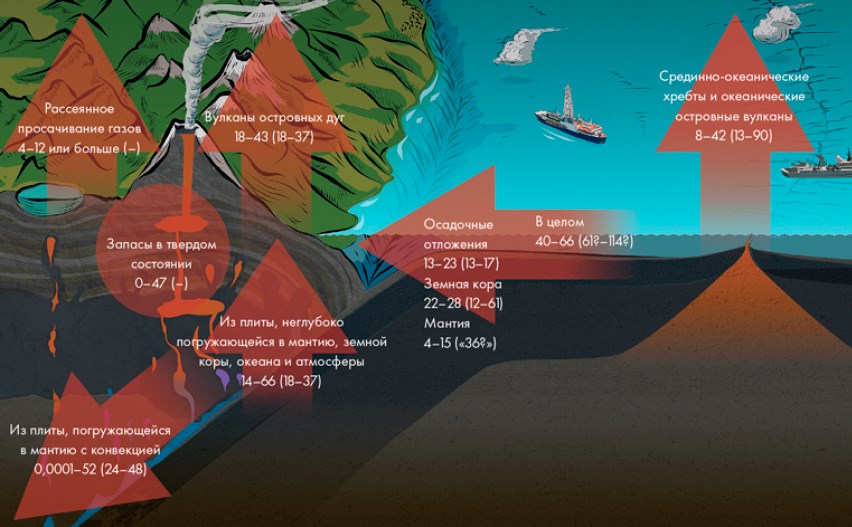 Глубинный углеродный цикл включает в себя резервуары и потоки углерода намного ниже поверхности Земли. Эти потоки показаны красными стрелками. Значения даны в мегатоннах углерода в год, в скобках приведены альтернативные цифры; (–) означает условия, для которых значения не определены. Рисунок из книги (с. 370)
Глубинный углеродный цикл включает в себя резервуары и потоки углерода намного ниже поверхности Земли. Эти потоки показаны красными стрелками. Значения даны в мегатоннах углерода в год, в скобках приведены альтернативные цифры; (–) означает условия, для которых значения не определены. Рисунок из книги (с. 370)
«Несмотря на жестко определенные физические, химические и биологические факторы, которые обусловливают большую часть минерального разнообразия нашей планеты, минералогия Земли уникальна для космоса», — автор «Симфонии № 6...» цитирует Грету Хистад, математика из Аризонского университета, чьи выводы опубликовал в 2015 году журнал Earth and Planetary Science Letters. Чтобы вычислить вероятность того, что две планеты будут иметь идентичную минералогию, она перемножила индивидуальные вероятности всех 5 000 минеральных видов. Оказалось, что вероятность несовпадения составила более 10320 (единица с 320 нулями).
«Химический состав планет имеет значение. Недавние исследования минералогов и геохимиков указывают на то, что даже небольшие отклонения в нем могут сделать планету непригодной для жизни. Если будет слишком много магния, не запустится движение плит — главный локомотив круговорота необходимых для жизни питательных веществ. Если не хватит железа — не сформируется магнитное поле, защищающее жизнь от смертоносных космических лучей. При недостаточном количестве воды, или углерода, или азота, или фосфора не зародится жизнь в той форме, которую мы знаем», — отмечает Роберт Хейзен.
Лимонная кислота начинает и выигрывает
Как неживые и «бесплодные» молекулы могут соединяться, самоорганизовываться, окружать себя защитными оболочками и — высший пилотаж — создавать собственные копии?
Это поступательное движение, последовательность химических шагов, с каждым из которых добавляется сложность структуры углеродсодержащей сети. Вот пример простейшего акта углеродной химии живой клетки — цикл лимонной кислоты (он же цикл Кребса, цикл трикарбоновых кислот). Этот цикл запускает энергетически насыщенная шестиуглеродная молекула лимонной кислоты, которая проходит десяток последовательных шагов фрагментации, сопровождаемых небольшим выделением поддерживающей клеточные функции энергии, а также созданием молекул, служащих отправной точкой для образования основных биохимических веществ. Этот основанный на углероде каскад химических реакций происходит триллионы раз в секунду.
Многие исследователи происхождения жизни считают, что цикл лимонной кислоты стал самой первой самовоспроизводящейся системой миллиарды лет назад. Действительным началом того, что называют жизнью, могла стать эта химическая инновация (или нечто подобное).
«Независимо от того, что стало этим стимулирующим фактором, — обратный цикл лимонной кислоты, самореплицирующаяся молекула РНК или какая-то другая самовоспроизводящаяся система, которую еще только предстоит описать, — спутанное сообщество молекул еле-еле взаимодействовало посредством этих замечательных новых способов. Но внезапно, в один момент непревзойденного творческого становления, это молекулярное сообщество начало создавать собственные копии».
Однако пока что никто не может понять, как произошло это преобразование, какие молекулы в нем участвовали и в какой последовательности они вступали в реакции друг с другом. И это, по мнению Роберта Хейзена, самый большой пробел в нашем понимании происхождения жизни:
«Кульминационный пункт моей любимой карикатуры Сидни Харриса, на которой длинное и сложное математическое доказательство <...> разбивается посередине фразой „Затем случилось чудо...”, а потом продолжается дальше».